AnYoNe
Member
Hallo zusammen,
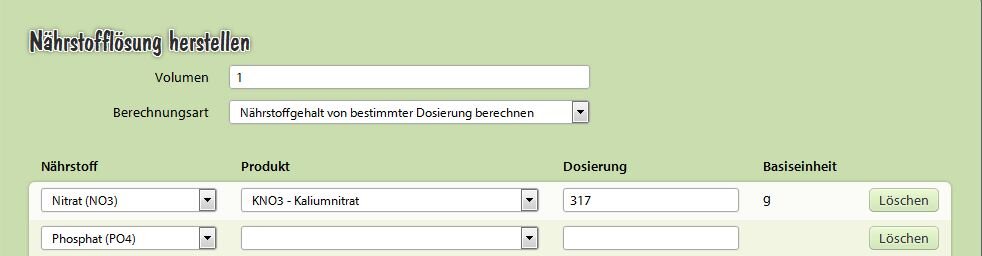
Eine Frage zum Nährstoffrechner - Nährstofflösung berechnen.
Habe hier im Forum unter Link gelesen, das daß Volumen die gesamte Menge incl. der Flüssigkeit und der Chemikalie sind.
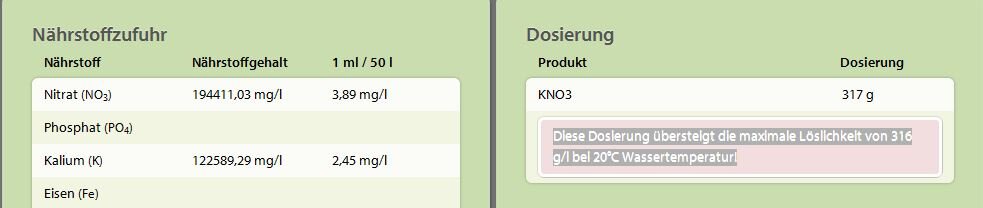
Allerdings wenn ich hier 317g KNO3 in einem Liter Wasser auflösen möchte, was die maximale Auflösung von 316 g pro Liter Wasser hat, kommt die Warnung "Diese Dosierung übersteigt die maximale Löslichkeit von 316 g/l bei 20°C Wassertemperatur! "
Das wiederspricht eigentlich der Aussage das das Volumen incl. Flüssigkeit und der Chemikalie ist. Da wie geschrieben es einen Liter Wasser braucht um 316g KNO3 zu aufzuösen.
Kann das jemand erklären?
Danke und Gruß Michl
Eine Frage zum Nährstoffrechner - Nährstofflösung berechnen.
Habe hier im Forum unter Link gelesen, das daß Volumen die gesamte Menge incl. der Flüssigkeit und der Chemikalie sind.
Allerdings wenn ich hier 317g KNO3 in einem Liter Wasser auflösen möchte, was die maximale Auflösung von 316 g pro Liter Wasser hat, kommt die Warnung "Diese Dosierung übersteigt die maximale Löslichkeit von 316 g/l bei 20°C Wassertemperatur! "
Das wiederspricht eigentlich der Aussage das das Volumen incl. Flüssigkeit und der Chemikalie ist. Da wie geschrieben es einen Liter Wasser braucht um 316g KNO3 zu aufzuösen.
Kann das jemand erklären?
Danke und Gruß Michl